식품의약품안전처는 동등생물의약품(바이오시밀러)의 품목허가 수수료 개편을 주요 내용으로 하는 '의약품 등의 허가 등에 관한 수수료 규정' 일부개정안을 11일 행정예고했다.

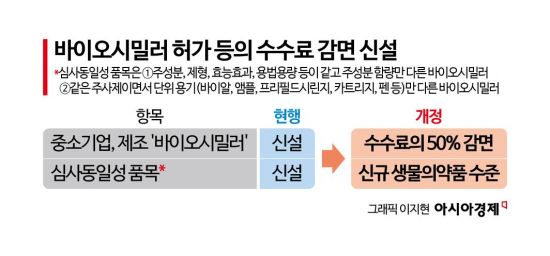
이번 행정예고는 지난 5일 진행한 부처 합동 '바이오 혁신 토론회' 후속 조치 중 하나로, 신약에 대한 수수료 개편 등 허가 혁신 방안을 동등생물의약품 허가에까지 적용해 허가 기간을 대폭 줄이기 위한 조치다.
동등생물의약품은 이미 제조판매·수입품목 허가를 받은 품목과 품질 및 비임상·임상적 비교동등성이 입증된 생물의약품을 일컫는다.
규정 개정안에 따르면 동등생물의약품의 품목허가 수수료가 현재 803만1000원에서 3억1000만원으로 재산정된다. 식약처는 관련 업계의 부담 완화를 위해 중소기업이 국내에서 개발한 동등생물의약품을 허가 신청한 경우 수수료의 50%를 감면하며, 동일 신청인이 유사한 허가를 신청한 경우에는 두 번째 품목부터 수수료를 800만원(전자민원 기준)으로 감면한다.
식약처는 수수료 인상에 따른 재원을 전담 심사팀 운영, 의·약사 같은 역량 높은 심사자 채용에 활용하는 등 심사역량 강화를 통해 현행 406일인 동등생물의약품 허가 기간을 내년부터는 295일까지 줄일 계획이다.
식약처는 "지난해 신약 허가 수수료 현실화에 이어 이번 동등생물의약품의 수수료 재산정을 통해 최근 급성장하는 바이오의약품에 대한 지원체계를 강화함으로써 해외 시장 진출을 앞당길 수 있을 것"이라고 기대했다.
개정안 내용은 식약처 홈페이지에서 확인할 수 있으면, 의견이 있는 경우 오는 11월11일까지 식약처로 제출하면 된다.
조인경 기자 ikjo@asiae.co.kr


![[포토] 예지원, 전통과 현대가 공존한 화보 공개](https://image.ajunews.com/content/image/2025/10/09/20251009182431778689.jpg)
![블랙핑크 제니, 최강매력! [포토]](https://file.sportsseoul.com/news/cms/2025/09/05/news-p.v1.20250905.ed1b2684d2d64e359332640e38dac841_P1.jpg)
![[포토] 발표하는 김정수 삼양식품 부회장](https://image.ajunews.com/content/image/2025/11/03/20251103114206916880.jpg)
![[포토]두산 안재석, 관중석 들썩이게 한 끝내기 2루타](https://file.sportsseoul.com/news/cms/2025/08/28/news-p.v1.20250828.1a1c4d0be7434f6b80434dced03368c0_P1.jpg)
![블랙핑크 제니, 매력이 넘쳐! [포토]](https://file.sportsseoul.com/news/cms/2025/09/05/news-p.v1.20250905.c5a971a36b494f9fb24aea8cccf6816f_P1.jpg)
![[포토] '삼양1963 런칭 쇼케이스'](https://image.ajunews.com/content/image/2025/11/03/20251103114008977281.jpg)
![[포토] 박지현 '순백의 여신'](http://www.segye.com/content/image/2025/09/05/20250905507414.jpg)
![[포토] 키스오브라이프 하늘 '완벽한 미모'](http://www.segye.com/content/image/2025/09/05/20250905504457.jpg)
![[포토] 아이들 소연 '매력적인 눈빛'](http://www.segye.com/content/image/2025/09/12/20250912508492.jpg)

![[포토] 국회 예결위 참석하는 김민석 총리](https://cphoto.asiae.co.kr/listimg_link.php?idx=2&no=2025110710410898931_1762479667.jpg)

![[포토] 박지현 '아름다운 미모'](http://www.segye.com/content/image/2025/11/19/20251119519369.jpg)
![[포토] 김고은 '단발 여신'](http://www.segye.com/content/image/2025/09/05/20250905507236.jpg)
![[작아진 호랑이③] 9위 추락 시 KBO 최초…승리의 여신 떠난 자리, KIA를 덮친 '우승 징크스'](http://www.sportsworldi.com/content/image/2025/09/04/20250904518238.jpg)
![[포토]첫 타석부터 안타 치는 LG 문성주](https://file.sportsseoul.com/news/cms/2025/09/02/news-p.v1.20250902.8962276ed11c468c90062ee85072fa38_P1.jpg)

![[포토] 알리익스프레스, 광군제 앞두고 팝업스토어 오픈](https://cphoto.asiae.co.kr/listimg_link.php?idx=2&no=2025110714160199219_1762492560.jpg)
![[포토] 키스오브라이프 쥴리 '단발 여신'](http://www.segye.com/content/image/2025/09/05/20250905504358.jpg)
![[포토]끝내기 안타의 기쁨을 만끽하는 두산 안재석](https://file.sportsseoul.com/news/cms/2025/08/28/news-p.v1.20250828.0df70b9fa54d4610990f1b34c08c6a63_P1.jpg)

![[포토] 한샘, '플래그십 부산센텀' 리뉴얼 오픈](https://image.ajunews.com/content/image/2025/10/31/20251031142544910604.jpg)
![[포토] 언론 현업단체, "시민피해구제 확대 찬성, 권력감시 약화 반대"](https://image.ajunews.com/content/image/2025/09/05/20250905123135571578.jpg)
![[포토] 김고은 '상연 생각에 눈물이 흘러'](http://www.segye.com/content/image/2025/09/05/20250905507613.jpg)
![[포토]두산 안재석, 연장 승부를 끝내는 2루타](https://file.sportsseoul.com/news/cms/2025/08/28/news-p.v1.20250828.b12bc405ed464d9db2c3d324c2491a1d_P1.jpg)
![[포토] 아홉 '신나는 컴백 무대'](http://www.segye.com/content/image/2025/11/04/20251104514134.jpg)

![[포토] TXT 범규 '반가운 손인사'](http://www.segye.com/content/image/2025/11/05/20251105518398.jpg)